| ||||||||
|
САНКТ-ПЕТЕРБУРГ | ||||||||
Мы приглашаем вас насладиться красками природы, посетив галерею фотографий.
Реклама |
комплексные поставки лакокрасочных материаловлаки, краски, эмали, грунтовки, шпатлевки |
|
Интересное обсуждение вопроса о том, являются ли линейные зависимости между энергиями Гиббса фундаментальными законами химии или же только эмпирическими правилами, имеющими ограниченную сферу применения, приведено в работах [126, 127]. Предпринимались попытки оценить два подхода к интерпретации линейных зависимостей между энергиями Гиббса исходя из практической применимости соответствующих моделей. Вольд и Сьёстрём [126] подчеркивали, что с точки зрения математики правильной представляется вторая интерпретация. Напротив, Тафт и Камлет [127] указывали, что с более приемлемой для химиков-экспериментаторов описательной точки зрения предпочтение следует отдать первой интерпретации. Однозначно ответить на этот вопрос пока что невозможно. Недавно опубликован обзор, в котором обсуждены эмпирические подходы к описанию влияния растворителей на химические процессы в растворах [289]. 7.2. Равновесные эмпирические параметры полярности растворителей Впервые попытка найти эмпирическую взаимосвязь между константой равновесия и полярностью растворителя была предпринята К. X. Мейером еще в 1914 г. [24]. Изучая влияние растворителей на кето-енольную таутомерию β-дикарбонильных соединений, он обнаружил, что константы таутомерного равновесия различных β-дикарбонильных соединений в одном ряду растворителей пропорциональны друг другу (см. табл. 4.2 в разд. 4.3.1). Наличие такой зависимости позволило рассматривать константу таутомерного равновесия Κτ как произведение двух независимых констант:
Здесь Ε — так называемая енольная постоянная, являющаяся мерой способности β-дикарбонилъного соединения к енолизации (по определению для этилацетата £=1); следовательно, так называемая десмотропная постоянная L — это мера енолизую щей способности растворителя. По определению L равно константе таутомерного равновесия этилацетата (£=1) в различных растворителях [24]. По-видимому, десмотропная постоянная была первым эмпирическим параметром растворителя, описывающим относительную эффективность сольватации дике тонного и енольного таутомеров β-дикарбонильных соединений. Десмотропная постоянная была определена только для нескольких растворителей и вскоре забыта. Указанному первому эмпирическому параметру растворителей можно противопоставить один из последних, предложенный Илиелом и Хоуфером в 1973 г. [25] и основанный на влиянии растворителей на конформационное равновесие 2-изопропил-5 метокси-1,3-диоксана (см. табл. 4.9 в разд. 4.4.3). В общем случае полярные растворители смещают это равновесие в сторону аксиального г ис-изомера, обладающего большим дипольным моментом. Связанное с этим равновесием стандартное изменение молярной энергии Гиббса — AG°och3 предложено называть параметром D\ (здесь D означает диоксан, а 1 — число атомов углерода в алкоксильной группе). Параметр D\ определен для 17 растворителей; его рекомендуют применять для оценки влияния растворителей на положение других равновесий и скорости различных реакций [25]. |
| ||||||||||||||||||||||||

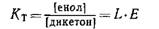 (7.9)
(7.9)