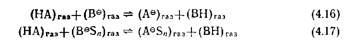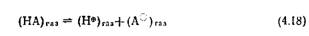| ||||||||
|
САНКТ-ПЕТЕРБУРГ | ||||||||
Мы приглашаем вас насладиться красками природы, посетив галерею фотографий.
Реклама |
комплексные поставки лакокрасочных материаловлаки, краски, эмали, грунтовки, шпатлевки |
|
В настоящее время определены кислотности и основность многих органических соединений в газовой фазе, чему способствовало освоение в течение последних 20 лет трех новых экспериментальных методов. К их числу относятся импульсная масс спектрометрия высокого давления (0,1—1300 Па) (МСВД) [22, 23, 118], послесвечение в быстром потоке газа, например гелия, при давлении около Ю-1—10~2 Па [119] и спектрометрия ионного циклотронного резонанса (ИЦР) с импульсным электронным пучком и ионной ловушкой, осуществляемая при давлении около 10~6—ΙΟ"3 Па [24—26, 115]. Разработка указанных методов изучения ионно-молекуляр ного равновесия коренным образом изменила состояние исследований в области кислотно-основных реакций в газовой фазе (и ряда других реакций; см. разд. 5.2). Теперь стало возможным сравнивать трудно объяснимые ситуации в растворах с простыми процессами в газовой фазе, а также определять в газовой фазе кислотность любых соединений — от самых слабых кислот типа метана до самых сильных. В растворах же в силу выравнивающего эффекта растворителя или низкой растворимости можно изучать только ограниченное число кислот. Путем измерения с помощью указанных выше методов констант равновесия К= [Αθ] [ВН]/[НА] [Βθ] реакций переноса протона типа реакции (4.16) удалось определить относительные собственные кислотности и основности молекул в газовой фазе. Результаты измерения аналогичных параметров реакций переноса протона типа реакции (4.17) (здесь S — молекула растворителя) позволяют оценить влияние растворителя при ступенчатой сольватации ионов, т. е. при последовательном присоединении молекул растворителя (η может изменяться от 0 до 4— 9), и тем самым изучать системы промежуточные между газофазными системами и растворами:
Стандартное изменение молярной энергии Гиббса в реакции (4.16) AG°——#Г1п К может служить мерой относительной кислотности НА и ВН (или относительной ооновности В® и Αθ). Путем изучения ряда кислот и оснований была составлена шкала относительной кислотности, аналогичная установленной ранее для величин р/<"а кислот в растворах. Кроме того, в результате изучения ряда стандартных реакций типа (4.18), например H2 H®-fHe или HF H®-(-F®, можно построить шкалу абсолютной собственной кислотности или основности, поскольку для таких реакций АН° и AS0 можно
рассчитать по имеющимся данным. Обычно абсолютную кислотность в газовой фазе выражают как сродство {РА) аниона А9 к протону, которое в свою очередь определяется как стандартное молярное изменение энтальпии АН° реакции депрото нирования в газовой фазе (4.18), т. е. 7Μ(ΑΘ) =—ΔН°. Для самых простых случаев в такой реакции энтропия AS0 изменяется примерно так же, и поэтому А#° (и AG°) приблизительно пропорциональны сродству к протону. |
| ||||||||||||||||||||||||