| ||||||||
|
САНКТ-ПЕТЕРБУРГ | ||||||||
Мы приглашаем вас насладиться красками природы, посетив галерею фотографий.
Реклама |
комплексные поставки лакокрасочных материаловлаки, краски, эмали, грунтовки, шпатлевки |
|
4.2. Влияние растворителей на кислотно-основное равновесие[1] 4.2.1. Кислоты и основания Бренстеда в растворах Как уже упоминалось в разд. 3.3.1, на равновесие ионизации кислоты [уравнение (4.5)] или основания [уравнение (4.6)] растворитель влияет не только в силу своей кислотности или основности, но и благодаря диэлектрической проницаемости, а также способности сольватировать нейтральные молекулы и ионы. (4.5)
Таким образом, изменение диэлектрической проницаемости или сольватирующей способности может влиять на кислотность кислоты НА или на основность основания А. Так, константа кислотности Ко карбоновых кислот в воде (ег = 78,3) примерно в 106 раз выше, чем в абсолютном спирте (ег=24,6), хотя вода всего лишь в 15—20 раз более сильное основание, чем этанол. Уравнение (4.5) описывает реакцию кислоты с амфипротон ным растворителем с образованием сольватированного протона и сопряженного с кислотой основания при их бесконечно большом удалении друг от друга. Часть энергии, необходимой для осуществления этой реакции, обеспечивается электростатическим взаимодействием между указанными ионами и может быть легко определена при помощи элементарной электростатической теории. Электростатическая работа, необходимая для переноса заряда к изолированным частицам НА, имеющим форму сферы радиусом Гн,\ π заряд ζΆκβ, в бесструктурной среде с диэлектрической проницаемостью &г выражается уравнением Борна:
где εο — диэлектрическая проницаемость вакуума, ζ — число элементарных зарядов е, Νχ—-число Авогадро [14]. Применение этого уравнения к кислотно-основному равновесию (4.5) приводит к уравнению (4.8), описывающему изменение энергии Гиббса в расчете на моль НА (при учете одного только электростатического взаимодействия) [8]: Следовательно, разность энергий Гиббса AAG ионизации 1 моля НА в растворителях 1 и 2 с диэлектрическими прони цаемостями er(i> и еГ(2> соответственно при условии, что радиусы молекул реагентов в растворителях 1 и 2 одинаковы, можно описать следующим уравнением:
Поскольку в соответствии с уравнением (4.3) изменение энергии Гиббса AG в реакции связано с константой равновесия Ка, то уравнение (4.9) можно преобразовать в уравнение:
Уравнение (4.10) справедливо только в том случае, если кислотность и основность растворителей 1 и 2 одинакова, поскольку в нем учтено только влияние диэлектрической проницаемости растворителя на степень ионизации. Если это условие соблюдено, то, согласно уравнению (4.10), логарифм константы ионизации /Са кислоты НА должен быть обратно пропорционален диэлектрической проницаемости растворителя, в котором она растворена. В силу указанных ограничений с помощью уравнения (4.10) можно получить только весьма приближенные количественные данные. Тем не менее это уравнение позволяет предсказать качественный характер влияния заряда кислоты на константу ее ионизации в растворителях с различной диэлектрической проницаемостью. |
| ||||||||||||||||||||||||

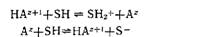 (4.6)
(4.6)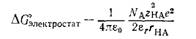 (4.7)
(4.7)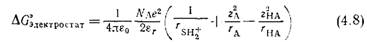
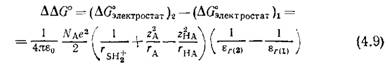
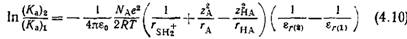 I
I