| ||||||||
|
САНКТ-ПЕТЕРБУРГ | ||||||||
Мы приглашаем вас насладиться красками природы, посетив галерею фотографий.
Реклама |
комплексные поставки лакокрасочных материаловлаки, краски, эмали, грунтовки, шпатлевки |
|
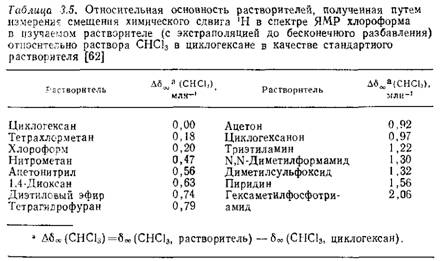
Недавно опубликованные результаты изучения реакций переноса протона в газовой фазе со ступенчатой сольватацией реагентов (т. е. с последовательным присоединением молекул растворителя, приводящим к образованию надмолекулярных кластерных соединений) показали, что по своим кислотно-основ
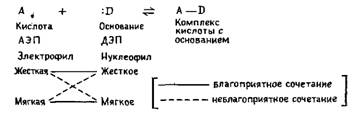
ным характеристикам изолированные молекулы могут резко отличаться от таких же молекул в жидкой фазе. Примером может служить вода — классический амфипротонный растворитель. В отличие от кислотно-основных свойств «полимерной» жидкой воды существующая в газовой фазе «мономерная» вода является более слабой кислотой и более слабым основанием, чем ее замещенные производные (R—ОН, R—О—R и т. п.), сопряженные кислотные или основные ионы которых стабилизированы за счет поляризации алкильных групп. Основность воды в газовой фазе приблизительно на 138 кДж-моль-1 (33 ккал· •моль-') ниже основности аммиака. Кислотность воды в газовой фазе сравнима с кислотностью пропилена и ниже кислотности фенола примерно на 167 кДж-моль-1 (40 ккал-моль-1). Если учесть хорошо известные кислотно-основные свойства воды, аммиака и фенола в водных растворах, нетрудно прийти к выводу, что различие между жидкой водой и изолированными газофазными молекулами воды должно быть связано с огромной энергией сольватации. Более подробно эта проблема рассматривается в разд. 4.2.2 и в приведенной там литературе. 3.3.2. Теория кислот и оснований Льюиса* В соответствии с теорией Льюиса кислотами являются акцепторы электронных пар (АЭП), а основаниями — доноры электронных пар (ДЭП), связанные следующим уравнением [63, 65а]:
Комплекс кислота Льюиса — основание Льюиса образуется за счет перекрывания занятой электронной парой орбитали донора D и вакантной орбитали акцептора А (см. также разд. 2.2.6). Такой подход к определению понятий кислота и основание был расширен Пирсоном, который разбил льюисовы кислоты и основания на две группы — жесткие и мягкие в зависимости от их электроотрицательности и поляризуемости (принцип жестких и мягких кислот и оснований; концепция ЖМКО) [66, 67]. Жесткие кислоты (например, Н®, Li®, Na®, BF3, А1С13, доноры водородных связей НХ) и жесткие основания (например, Р9, С1®, НО®, RO®, Н20, ROH, R20, NH3) обычно построены из сильно электроотрицательных и обычно слабополяризуемых небольших атомов. Мягкие кислоты (например, Ag®, Hg®, I2> 1,3,5-тринитробензол, тетрацианэтилен) и мягкие основания (например, Н®, Iе, R®, RS®, RSH, R2S, алкены, С6Нб) обычно содержат большие атомы, обладают слабой электроотрицательностью и, как правило, легко поляризуются. Такое разделение позволяет прийти к простому правилу, устанавливающему устойчивость комплексов кислота Льюиса — основание Льюиса: жесткие кислоты предпочтительно связываются с жесткими основаниями, а мягкие кислоты — с мягкими основаниями [66, 67]. Это правило (концепция ЖМКО) качественно хорошо описывает большое число химических явлений и широко используется в органической химии [66—70] (критику концепции ЖМКО см. в работах [71, 72]). Недавно Пирсон опубликовал о&зор, посвященный успехам концепции ЖМКО и ее теоретическому подтверждению [170]. Основываясь на величинах потенциала ионизации и сродства к электрону, различным кислотам ,и основаниям Льюиса сейчас можно даже приписать определенные численные значения абсолютной жесткости, т. е. устойчивости к деформации или изменению электронного облака частицы. |
| ||||||||||||||||||||||||||