| ||||||||
|
САНКТ-ПЕТЕРБУРГ | ||||||||
Мы приглашаем вас насладиться красками природы, посетив галерею фотографий.
Реклама |
комплексные поставки лакокрасочных материаловлаки, краски, эмали, грунтовки, шпатлевки |
|
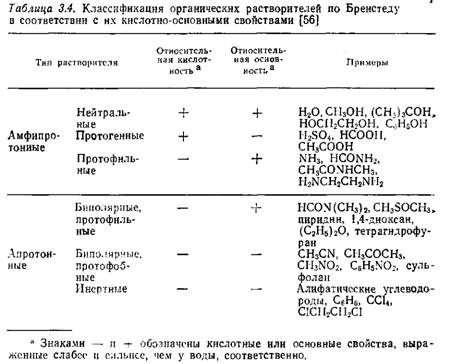
Описанная выше классификация растворителей впервые была предложена Бренстедом, разбившим растворители на 4 класса в соответствии с их кислотно-основными свойствами [54]. Эта классификация была несколько уточнена Дэйвисом, который учитывал еще диэлектрическую проницаемость растворителей (больше 20 и меньше 20) и получал таким путем 8 классов растворителей {47]. В слегка упрощенном Кольтгофом виде эта классификация приведена в табл. 3.4 [56]. Вода представляет собой прототип амфипротонных растворителей, а все другие растворители с близкими кислотно-основны ми характеристиками называют нейтральными. Растворители, представляющие собой по сравнению с водой значительно более сильные кислоты и гораздо более слабые основания, называют протогенными; если же растворитель является более сильным основанием и более слабой кислотой, чем вода, то его называют мротофильным. Такое разделение растворителей в известной мере искусственно, поскольку стандартный растворитель — вода — нейтрален по определению. Из уравнения (3.8) следует, что степень ионизации кислоты зависит от основности растворителя. Другими словами, эффективная сила кислоты тем выше, чем выше сродство среды к протону. Однако ионизация кислоты определяется не только основностью растворителя, но и его диэлектрической проницаемостью и способностью сольватировать ионы. Зависимость констант кислотности и основности соединений от основности ή кислотности растворителя соответственно позволяет разделить растворители на выравнивающие и дифференцирующие [49, 57, 58]. Все неорганические кислоты в водных растворах ионизируются в одинаковой степени; точнее, в силу практически количественно протекающей реакции с водой как с основанием они ионизируются практически полностью. Однако было бы довольно странным, если бы сила всех этих кислот была одинаковой независимо от их химической природы. Этот факт можно объяснить выравнивающим влиянием воды на силу кислот.
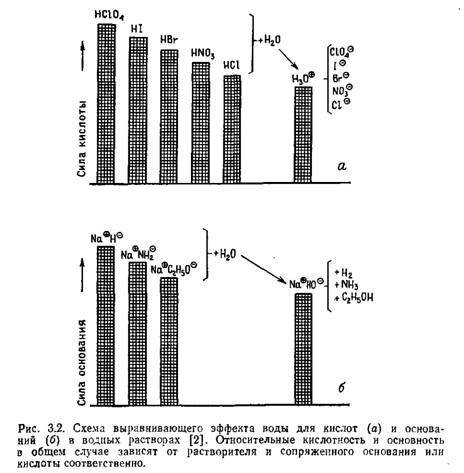
На рис. 3.2 приведены данные, показывающие, что в воде сила любой кислоты не превосходит силу Н3О+ Обладающие такими свойствами растворители называют выравнивающими*. Для того чтобы оценить относительную силу минеральных кислот, необходимо производить измерения в растворителях с очень низкими основностью и ионизирующей способностью. По понятной причине такие растворители назвали дифференцирующими. Приведенная на рис. 3.2 диаграмма показывает, что в раствори-
теле SH сильнейшими кислотой и основанием являются ион лиония SHz® (Н30® в случае воды) и лиат-ион S® (НО® в случае воды) соответственно. Так, в метаноле хлороводород полностью ионизирован, а азотная кислота только частично. В менее основной муравьиной кислоте хлороводород также ионизирован только частично, тогда как первый протон молекулы серной кислоты все еще ионизирован полностью. Ацетони трил представляет собой очень слабое основание и чрезвычайно слабую кислоту, и поэтому в нем наблюдается лишь небольшое выравнивание силы кислот и оснований, т. е. он — хороший дифференцирующий растворитель. Действительно, в ацетонитри ле HCIO4 является сильной кислотой, а сила других кислот убы- |
| ||||||||||||||||||||||||||