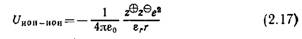| ||||||||
|
САНКТ-ПЕТЕРБУРГ | ||||||||
Мы приглашаем вас насладиться красками природы, посетив галерею фотографий.
Реклама |
комплексные поставки лакокрасочных материаловлаки, краски, эмали, грунтовки, шпатлевки |
|
Измерением электропроводности можно отличить свободные ионы от ассоциированных ионов и ковалентных молекул, поскольку только свободные ионы обеспечивают электропроводность растворов [136]. Спектрофотометрия позволяет отличить свободные ионы и ионные пары от ковалентно связанных молекул, поскольку в первом приближении спектроскопические характеристики ионов не зависят от степени их ассоциации с противоионами [141]. Затем, воспользовавшись уравнением (2.16), можно выразить найденную путем измерения электропроводности константу равновесия Лэксп через константы ионизации и диссоциации. Если степень ионизации мала, то Кэксп = Кдисс· Растворители влияют на обе стадии, описываемые уравнением (2.13), ионизацию и диссоциацию, но различными путями. Согласно уравнению (2.17), сила электростатического притяжения между двумя противоположно заряженными ионами обратно пропорциональна диэлектрической проницаемости растворителя. Следовательно, только растворители с достаточно высокой диэлектрической проницаемостью способны снизить сильное электростатическое взаимодействие между ионами с разноименными зарядами до такой степени, чтобы ионные пары смогли диссоциировать на свободные сольватированные ионы. Такие растворители обычно называют диссоциирующими растворителями*. Электростатическое взаимодействие между ионами с разноименными зарядами может быть преодолено только при достаточно высокой стандартной молярной энергии Гиббса сольватации АССОльв.
(Здесь Uиои-ион — потенциальная энергия ион-ионного взаимодействия, ze— заряд иона, г — расстояние между ионами, εο и гг — диэлектрическая проницаемость вакуума и среды соответственно.) В водных растворах в силу чрезвычайно высокой диэлектрической ' проницаемости воды (εΓ = 78,3) ассоциация ионов наблюдается только при очень высоких концентрациях. Напротив, в растворителях с диэлектрической проницаемостью менее 10—15 свободные ионы практически не обнаружены (например, в углеводородах, хлороформе, 1,4-диоксане, уксусной кислоте). Если же диэлектрическая проницаемость растворителя превышает 40, то в таких растворителях ионы практически не ассоциированы (например, в воде, муравьиной кислоте, формамиде). В растворителях с умеренной диэлектрической проницаемостью (εΓ=15—20; например, в этаноле, нитробензоле, ацетонитриле, ацетоне, Ν,Ν-диметилформамиде) соотношение свободных и ассоциированных ионов зависит от природы как растворителя, так и электролита, в том числе от величины иона, степени дело кализации заряда, наличия связанных водородными связями ионных пар, специфической сольватации ионов и т. п. ([96]. Так, галогениды лития в ацетоне (εΓ = 20,7) являются очень слабыми электролитами, в то время как галогениды тетраалки ламмония в том же растворителе сильно диссоциированы ;[142— 144]. Определение констант ассоциации в растворителях с очень низкой диэлектрической проницаемостью типа бензола (ег= = 2,3) обычно приводит к очень большим величинам. Это свидетельствует о том, что в таких растворителях большинство ионных пар группируется в еще более сложные структуры [96]. |
| ||||||||||||||||||||||||

 Д9ксп=ЛионЛдисс (при Хион«1 или [Α®Βθ]«ίΟ). В случае сильных электролитов, у которых Кион>1, уравнение (2.16) упрощается до выражения
Д9ксп=ЛионЛдисс (при Хион«1 или [Α®Βθ]«ίΟ). В случае сильных электролитов, у которых Кион>1, уравнение (2.16) упрощается до выражения