| ||||||||
|
САНКТ-ПЕТЕРБУРГ | ||||||||
Мы приглашаем вас насладиться красками природы, посетив галерею фотографий.
Реклама |
комплексные поставки лакокрасочных материаловлаки, краски, эмали, грунтовки, шпатлевки |
|
Многие макромолекулярные соединения лучше растворяются в смесях растворителей, чем в соответствующих чистых растворителях [20]. Так, поливинилхлорид нерастворим ни в ацетоне, ни в дисульфиде углерода, но растворяется в их смеси. Известны и противоположные эффекты. Например, полиакри лонитрил растворяется как в малодинитриле, так и в Ν,Ν-ди метилформамиде, но не в их смеси [20]. При комнатной температуре мыла не растворяются ни в этиленгликоле, ни в углеводородах, но растворяются в смеси этих веществ, в которой этиленгликоль сольватирует ионный центр молекулы, а углеводород неполярную цепь жирной кислоты ,[128]. Предпринималось несколько попыток создать модели, удовлетворительно описывающие избирательную сольватацию ионов и нейтральных молекул на количественном уровне [120, 257— 261]. Одна из них, названная теорией конкурентной предпочтительной сольватации (COPS-теория; от английского competitive preferential solvation theory), успешно применялась для описания многих физико-химических свойств веществ в смесях растворителей [258]. 2.5. Мицеллярная сольватация (солюбилизация)* В растворах больших катионов и анионов с длинными неразвет вленными углеводородными цепями, например СН3(СН2)П· •С02еМ®, СН3— (СН2) η—S03eM® или СНз(СН2)„Ы(СНз)3вХе (л>7),_ создаются специфические условия. Такие соединения называют амфифильными, подразумевая, что в их молекулах
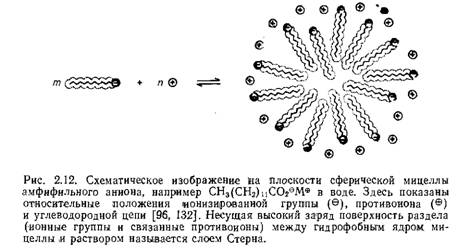
имеются как полярные, так и неполярные группировки. В разбавленных водных растворах соли таких больших органических ионов часто образуют ассоциаты. Ассоциаты указанного типа, обладающие упорядоченным строением, вместе с ионами, локализующимися на их периферии за счет сил электростатического притяжения, называют мицеллами**. На рис. 2.12 схематично изображен процесс образования сферической мицеллы из амфи фильных анионов. Гидрофобные группировки ассоциированных молекул образуют ядро мицеллы, а ионизированные группы располагаются на границе раздела мицеллы с водой и контактируют с молекулами воды. В воде такие мицеллы обычно имеют средний радиус 2—4 нм и состоят из 50—100 мономерных молекул [132]. Их форма обычно близка к сферической или эллипсоидной. В неводных неполярных растворителях мицеллы обычно имеют обратную структуру, т. е. ионные группы образуют ядро мицеллы, и углеводородные цепи ионов контактируют с неполярным растворителем [132]. В очень разбавленных растворах амфифильные ионы ведут себя как обычные сильные электролиты, но если их концентрация превышает так называемую критическую концентрацию мицеллообразования (ккм), обычно равную 10~4—10~2 моль· •л-1, то образуются сферические ассоциаты. Принято считать, что движущей силой образования мицелл являются три типа межмолекулярных взаимодействий: гидрофобное отталкивание между углеводородными цепями и водным окружением (см. разд. 2.2.7), отталкивание одноименно заряженных ионных групп тг~~вандерваальсово притяжение между алкильными цепями (обычно неразветвленными цепями, содержащими от 8 до 18 атомов углерода). |
| |||||||||||||||||||||||||