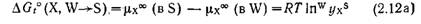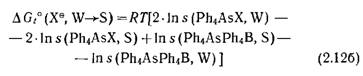| ||||||||
|
САНКТ-ПЕТЕРБУРГ | ||||||||
Мы приглашаем вас насладиться красками природы, посетив галерею фотографий.
Реклама |
комплексные поставки лакокрасочных материаловлаки, краски, эмали, грунтовки, шпатлевки |
|
Непосредственной мерой энергии сольватации иона, несомненно, является стандартная молярная энергия Гиббса сольватации, т. е. переноса этого иона из газовой фазы в раствор (рис. 2.8). Этот параметр, однако, обычно неизвестен, особенно если речь идет о неводных растворителях. Поэтому вместо АСсольв обычно с неменьшим успехом применяют другой параметр — стандартную молярную энергию Гиббса переноса иона X из воды W (стандартного растворителя) в другой растворитель S; этот параметр, обозначаемый ΔGt°(X, W-»-S), определяется следующим уравнением:
Здесь μχ°° — стандартный (т. е. относящийся к бесконечному разбавлению) химический потенциал X, a wyxs — так называемый коэффициент активности переноса X из W в S. Для того чтобы вычислить ΔG°(X, W-»-S) индивидуальных ионов по экспериментальным данным, относящимся к истинным электролитам, было принято допущение,. что AGi°(Ph4As®, W->-S) = = AGf°(Ph4Be, W-»-S) для всех растворителей, если в качестве стандартного электролита использовать Ph4As®Ph4Be (Ph = = СбН5). Это допущение представляется достаточно обоснованным, поскольку большие симметричные ионы тетрафенилбора та тетрафениларсония имеют сравнимые размеры, структуры и заряды и, следовательно, сольватируются примерно одинаково при переходе от одного растворителя к другому. Опубликованы обзоры, в которых обсуждены доводы за и против такого допущения [235, 241, 243, 244]*. Экспериментально молярную энергию Гиббса переноса аниона Xе рассчитывают по результатам четырех экспериментов определения растворимости солей Ph4As®Ph4Be и Ph4As®Xe вводе (W) и в растворителе (S). Тогда энергия Гиббса переноса равна Здесь s — растворимость, выраженная в молях на литр (моль· л-1). В табл. 2.9 приведен ряд величин AG°(X, W- S), найденных описанным путем; эти данные заимствованы из подробного критического обзора Маркуса [244]. В работе Перссона [301] представлены графики зависимостей изменения ΔG°, АН° и ΔSt° при переносе однозарядных простых ионов из воды в другие растворители. Далее эта проблема обсуждается в разд. 5.5.3. В процессах сольватации важно принимать во внимание стехиометрию сольватных комплексов (которая обычно описывается координационным числом или числом сольватации), лабильность сольватных комплексов (обычно описываемую как скорость обмена сольватированных молекул с несольватирован ными), а также тонкую структуру сольватной оболочки (которая в случае воды часто хорошо описывается простой моделью сольватации нона, предложенной Франком и Веном [16]). |
| ||||||||||||||||||||||||