| ||||||||
|
САНКТ-ПЕТЕРБУРГ | ||||||||
Мы приглашаем вас насладиться красками природы, посетив галерею фотографий.
Реклама |
комплексные поставки лакокрасочных материаловлаки, краски, эмали, грунтовки, шпатлевки |
|
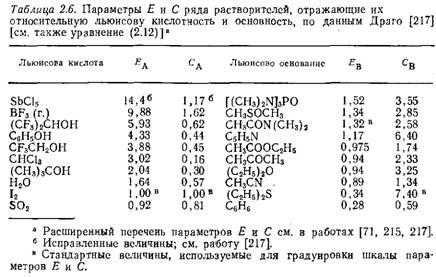
Первоначально значения Ε и С для ряда растворителей определяли главным образом путем измерения энтальпии образования аддуктов иода и фенола (в качестве акцепторов электронов) с алкиламинами (в качестве доноров электронов). Позднее уточненные величины Ε и С вычисляли с помощью ЭВМ путем оптимизации обширной базы данных, включающей величины энтальпии указанных процессов и четырех произвольно выбранных фиксированных стандартных значений параметров, в том числе £'а=Са=1 для иода, £в=1,32 для Ν,Ν-диметилацет амида и Св = 7,40 для диэтилсульфида [71, 215]. В табл. 2.6 приведены параметры Ε и С для некоторых льюисовых кислот и оснований, обычно используемых в качестве растворителей. На основании этих параметров можно с удивительной точностью предсказывать энтальпии реакций между кислотой и основанием Льюиса (±0,8 кДж-моль-1) даже в тех случаях, когда соответствующие реакции невозможно осуществить экспериментально [216]. Опубликованы результаты сравнения свойств растворителей, оцененные методом Драго на основе параметров £ и С и методом Гутманна [53, 67], на базе донорных чисел [200, 217, 218]. Предложено модифицированное уравнение типа уравнения (2.12), учитывающее специфические и неспецифические взаимодействия между растворенными веществами и полярными растворителями [219]. В заключение следует отметить, что предпринимались попытки оценить электронодонорные и электроноакцепторные свойства органических растворителей с помощью спектроскопии ЯМР Ή [73] и ИК-спектроскопии [72, 73]. Другие эмпирические параметры льюисовой кислотности и основности обсуждены в разд. 7.2—7.5. 2.2.7. Сольвофобные взаимодействия* Растворимость углеводородов в воде чрезвычайно низка. Поэтому растворение углеводорода в воде обычно сопровождается повышением энергии Гиббса G системы (AG>0). Экспериментально установлено, что растворение углеводородов в воде представляет собой экзотермический процесс (Д#<0); поскольку AG = AH—Τ AS, отсюда следует, что энтропия системы
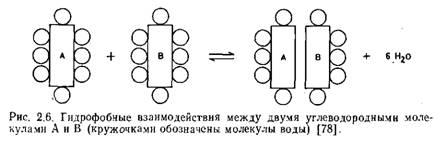
должна уменьшаться. Этот факт можно интерпретировать как следствие высокоупорядочеииого расположения молекул воды вокруг растворенных углеводородных молекул. Другими словами, вблизи от растворенных молекул углеводородов молекулы воды упакованы плотнее, чем в чистой воде. Такой эффект называют также совершенствованием структуры. При смешении водных растворов двух углеводородов последние могут образовывать ассоцнат с одновременным переходом части молекул воды в первоначальное менее упорядоченное состояние. Этот процесс схематично представлен на рис. 2.6. |
| ||||||||||||||||||||||||||