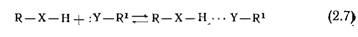| ||||||||
|
САНКТ-ПЕТЕРБУРГ | ||||||||
Мы приглашаем вас насладиться красками природы, посетив галерею фотографий.
Реклама |
комплексные поставки лакокрасочных материаловлаки, краски, эмали, грунтовки, шпатлевки |
|
Член а2 в уравнении (2.66) свидетельствует о быстром усилении дисперсионного взаимодействия при увеличении объема молекулы и числа поляризуемых электронов. В соответствии с уравнением Лоренца — Лорентца поляризуемость а связана с молекулярной рефракцией и с показателем преломления. Таким образом, растворители с большим показателем преломления и, следовательно, с большой оптической поляризуемостью должны проявлять особенно сильные дисперсионные взаимодействия. Как указано в табл. А.1 (см. приложение) все ароматические соединения обладают сравнительно высокими показателями преломления (п= 1,6273, 1,6200, 1,5863 и 1,5763 для хино лина, иодбензола, анилина и дифенилового эфира соответственно), а из всех органических растворителей наибольший показатель преломления (п—1,6280) имеет дисульфид углерода. Растворители с высокой поляризуемостью часто хорошо сольватируют анионы, если последние также обладают высокой поляризуемостью. Это обусловлено усилением дисперсионных взаимодействий между молекулами растворителя и большими поляризуемыми анионами типа 1зе, Iе, SCN® или пикрата в отличие от меньших анионов, например F®, НО® или I N® [36]. Необычно низкие температуры кипения фторуглеводородов обусловлены слабой поляризуемостью электронов, прочно удерживаемых ядром атома фтора. . 2.2.5 Водородные связи* Жидкости, в молекулах которых имеются гидроксильные или другие группы, построенные из атома водорода и связанного с ним электроотрицательного атома X, сильно ассоциированы и имеют аномально высокие температуры кипения. Этот факт свидетельствует о наличии межмолекулярных взаимодействий особого рода, получивших название водородных мостиков или водородных связей, где атом водорода имеет координационное число 2. В общем случае водородную связь определяют следующим образом: если ковалентно связанный атом водорода образует еще одну связь с другим атомом, то вторую связь называют водородной [44]. Понятие о водородной связи ввел в 1919 г. Хаггинс [41]. Первая важная работа по изучению водородных связей (в применении к ассоциации молекул воды) была опубликована & 1920 г. Латимером и Роудбушем [191]. Все три упомянутых исследователя тогда работали в лаборатории Дж. Н. Льюиса (Калифорнийский университет, Беркли, США). Водородная связь образуется в результате взаимодействия молекул R—X—Η и :Y—R1 в соответствии с уравнением
Здесь R—X—Η — донор протонов, a :Y—R! — источник электронной пары, необходимой для создания мостиковой связи. Таким образом, образование водородной связи можно рассматривать как стадию, предшествующую реакции между бренсте довой кислотой и бренстедовым основанием, в результате которой образовывался бы биполярный продукт типа R—ΧΘ···Η— —Υ®—R1. Атомы X и Υ должны быть более электроотрицательными, чем атом водорода (например, С, Ν, Р, О, S, F, CI, Вг„ I). Водородные связи могут быть как межмолекулярпыми, так и внутримолекулярными; в последнем случае X и Υ принадлежат одной молекуле. |
| ||||||||||||||||||||||||