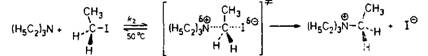| ||||||||
|
САНКТ-ПЕТЕРБУРГ | ||||||||
Мы приглашаем вас насладиться красками природы, посетив галерею фотографий.
Реклама |
комплексные поставки лакокрасочных материаловлаки, краски, эмали, грунтовки, шпатлевки |
|
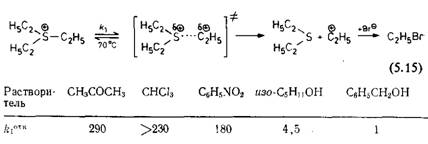
Скорость сольволиза солей грет-бутилдиметилсульфония снижается при повышении полярности растворителя [710]. Аналогично скорость сольволиза солей триэтилоксония в водном этаноле снижается при повышении содержания воды [490]. Скорость сольволиза солей N-грег-алкилпиридиния, например перхлората 1-(1-метил-1-фенилэтил)пиридиния, почти не зависит от полярности растворителя, в то время как сольволиз солей iV-вгор-алкилпиридиния незначительно замедляется при повышении полярности растворителя [710]. Так как в реакциях типа б (см. табл. 5.4) на стадии образования активированного комплекса заряда не возникает, то на скорость таких реакций полярность растворителя влияет в гораздо меньшей степени. Примером реакций типа в (табл. 5.4) может служйть хорошо известная реакция Меншуткина между третичными аминами и первичными галогеналканами с образованием четвертичных солей аммония [30]. Зависимость таких реакций от природы растворителя тщательно изучалась несколькими группами исследователей [51—65, 491—496]. Например, реакция три м-пропиламина с иодметаном при 20 °С в диэтиловом эфире1 хлороформе и нитрометане соответственно в 120, 13 000 и 110 000 раз быстрее, чем в м-гексане [60]. Рассчитано, что активированный комплекс, образующийся в этой реакции, должен иметь дипольный момент около 29· Ю-30 Кл-м (8,7 Д) [23, 64], что значительно больше суммарного дипольного момента исходных веществ (2,3· Ю-30 Кл-м или 0,70 Д и 5,5· 10~30 Кл-м или 1,64 Д для три-м-пропиламина и иодметана соответственно) [64].
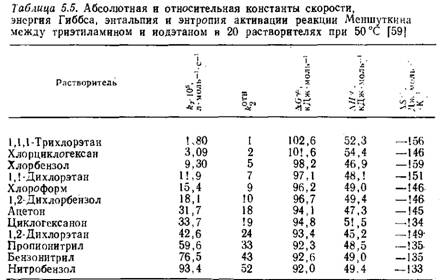
Опубликованы данные о зависимости параметров активации реакции триэтиламина с иодэтаном от растворителя [59]. Скорость этой реакции в полярных апротонных растворител5/х, а также соответствующие параметры активации приведены в табл. 5.5 [59]. (5.16)
Замена 1,1,1-трихлорэтана в качестве растворителя на нитробензол сопровождается ускорением реакции (5.16) в 52 раза, что соответствует уменьшению на 10,6 кДж-моль-1. Для бимолекулярных реакций типа (5,16), в которых заряды возникают в процессе активации, обычно характерны большие отрицательные величины энтропии активации. Отрицательная энтропия активации свидетельствует о большей упорядоченности в переходном состоянии по сравнению с начальным состоянием системы, что обусловлено более эффективной сольватацией активированного комплекса по сравнению с исходными веществами. Приведенные в табл. 5.5 данные показывают, что наибольшее снижение энтропии активации ASф характерно для реакции в менее полярных растворителях. Этот факт можно объяснить более упорядоченной структурой полярных растворителей, молекулы которых связаны друг с другом за счет межмолекулярных взаимодействий. Молекулы менее полярных растворителей, имеющие небольшой или равный нулю дипольный момент, сравнительно плохо ориентированы относительно друг друга и поэтому обладают более высокой энтропией. Повышение степени сольватации активированного комплекса приводит к сильному снижению энтропии в неполярных растворителях, поэтому и реакции, в ходе которых образуются биполярные активированные комплексы, будут иметь большую (по абсолютной величине) отрицательную энтропию активации в менее полярных растворителях [226]. |
| ||||||||||||||||||||||||||